Effective Nuclear Charge in Hindi प्रभावी नाभिकीय आवेश क्या है समझाइए
[wpsm_titlebox title=”Contents” style=”1″][contents h2 h3 h4][/wpsm_titlebox]
प्रभावी नाभिकीय आवेश (Effective Nuclear Charge)
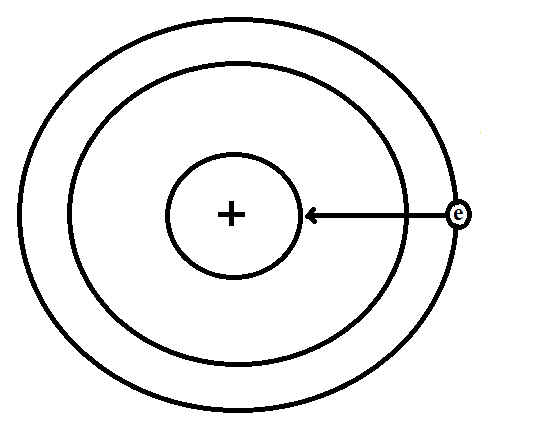
किसी परमाणु के नाभिक के द्वारा बाह्यतम कोश में उपस्थित इलेक्ट्रॉनों पर लगाया जाने वाला आकर्षण बल प्रभावी नाभिकीय आवेश (Effective Nuclear Charge) कहलाता है।
बहुइलेक्ट्राॅनीय परमाणु (Polyelectronic atom) में ENC
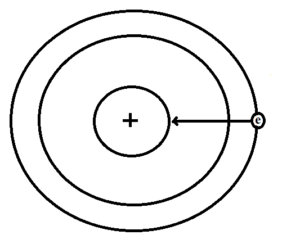
किसी भी बहुइलेक्ट्राॅनीय परमाणु (Polyelectronic atom) में आन्तरिक इलेक्ट्राॅन, बाह्यतम कोश के इलेक्ट्राॅनों को प्रतिकर्षित करते हैं तथा इस प्रतिकर्षण (repel) के कारण बाह्यतम कोश के इलेक्ट्राॅन पर नाभिकीय आकर्षण (nuclear attraction) कम हो जाता है।
अतः बाह्यतम कोश के इलेक्ट्राॅन पर नाभिकीय आवेश का एक हिस्सा ही प्रभावी होता है। इस प्रकार अन्दर वाले इलेक्ट्राॅन अपने नाभिक का परिरक्षण करके, नाभिकीय आवेश को बाह्यतम कोश के इलेक्ट्राॅन के प्रति कम कर देते है।
अतः नाभिकीय आवेश का वह भाग, जो बाहरी इलेक्ट्राॅन का कार्य करता है, प्रभावी नाभिकीय आवेश कहलाता है
Zeff=Z-σ
यहाँ
Zeff = प्रभावी नाभिकीय आवेश (effective nuclear charge)
σ = परिरक्षण नियतांक (shielding constant)
Z = नाभिकीय आवेश (nuclear charge)
p – ब्लॉक तत्व (p – block element)
परिरक्षण नियतांक (shielding constant)
स्लेटर ने परिरक्षण नियतांक (shielding constant) ज्ञात करने के कुछ नियम बनाये जो निम्नलिखित है –
- 1s कक्षक के एक इलेक्ट्राॅन का परिरक्षण प्रभाव (shielding effect or secreening effect) 0.30 होता है।
- ns तथा np अर्थात् बाह्यतम कोश में उपस्थित प्रत्येक इलेक्ट्राॅन का परिरक्षण प्रभाव (shielding effect or secreening effect) 0.35 होता है।
- उपान्त्य कोश (penultimate orbit) (n-1) के s, p और d कक्षकों में प्रत्येक इलेक्ट्राॅन का परिरक्षण प्रभाव (shielding effect or secreening effect) 0.85 होता है।
- पूर्व उपान्त्य कोश (prepenultimate orbit) (n-2) के एवं उसके नीचे के सभी s, p, d और f कक्षकों में उपस्थित प्रत्येक इलेक्ट्राॅन का परिरक्षण प्रभाव (shielding effect or secreening effect) 1.0 होता है। इन्हीं नियमों से हम किसी भी परमाणु का प्रभावी नाभिकीय आवेश ज्ञात करते है।
परमाणु का आकार और प्रभावी नाभिकीय आवेश में सम्बन्ध
प्रोटोन की संख्या में वृद्धि होने के कारण प्रभावी नाभिकीय आवेश (Effective Nuclear Charge) को बढ़ाता है, फलस्वरूप प्रोटोन इलेक्ट्रोनिक कोशों को नाभिक की और अधिक बल से आकर्षित करते हैं।
जिससे परमाणवीय त्रिज्या (ATOMIC RADIUS) कम होती है। और परमाणु का आकार घटता है।
आधुनिक आवर्त सारणी और प्रभावी नाभिकीय आवेश
एक आवर्त में बाएं से दाएं जाने पर बाह्यतम कोश में इलेक्ट्रॉनों की संख्या बढ़ती है। जिसके कारण वह नाभिक की ओर अधिक आकर्षित होता है। अतः प्रभावी नाभिकीय आवेश (Effective Nuclear Charge) को बढ़ता है।
एक वर्ग मेंऊपर से नीचे की ओर आने इलेक्ट्रॉनिक कोशों की संख्या बढ़ती है। जिसके कारण उसका नाभिक की ओर आकर्षण कम होता जाता है। अतः प्रभावी नाभिकीय आवेश (Effective Nuclear Charge) को घटता है।
इन्हें भी पढ़े
- तत्वों का वर्गीकरण एवं आधुनिक आवर्त सारणी (Classification of elements and modern periodic table)
- नाइट्रोजन एवं इसके यौगिक के भौतिक एवं रासायनिक गुणधर्म (Physical and chemical properties of nitrogen and its compound)
बाहरी कड़ियाँ
- https://www.aliseotools.com/en/backlink-checker
- https://www.aliseotools.com/en/alexa-rank-checker
- https://www.aliseotools.com/en/word-counter
- https://amzn.to/2QJep7W
- https://amzn.to/3aokpJZ